※ この記事はAging Loop Matrix® 2.0(ALM 2.0)の拡張因子シリーズです。ALMコア11因子については#01〜#11をご覧ください。
🧑💼 お客様への伝え方
ロンジェビティ医療は「病気になる前」の健康な方を対象とした予防医療です。このセクションは、外来でお客様にこのループをわかりやすく伝えるための言葉の例です。専門用語を避け、日常のイメージで伝えることを意識しています。そのままお使いいただくか、先生ご自身の言葉にアレンジしてご活用ください。
染色体の端には「保護キャップ」がある
靴ひもの端にはほつれを防ぐプラスチックのキャップがついています。私たちの染色体の端にも、同じような役割を果たす「テロメア」という構造があります。テロメアは染色体末端を保護し、遺伝情報が傷つかないように守っています。
しかし細胞が分裂するたびに、このテロメアは少しずつ短くなります。これは避けられない生命の仕組みです。そして、テロメアが限界まで短くなると、細胞は「これ以上分裂してはいけない」というシグナルを受け取り、活動を停止します。これが「複製老化」です。
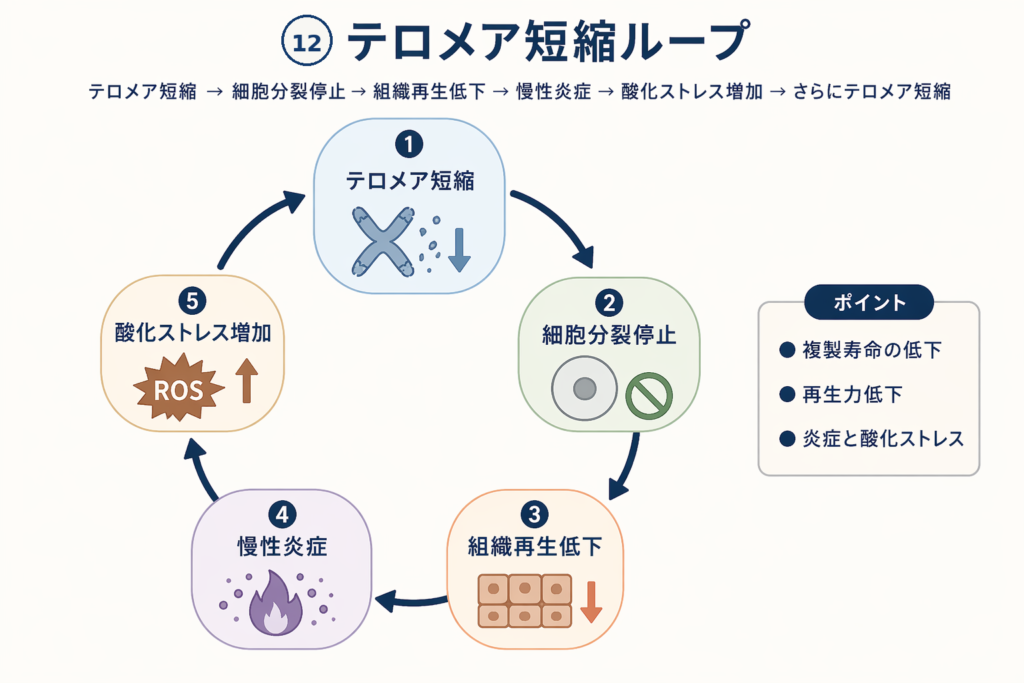
問題は、このテロメア短縮が悪循環を作り出すことです:
- テロメアが短くなる → DNA損傷シグナルが発動する
- 細胞老化(Senescence)が起きる → SASPが分泌される
- SASPが慢性炎症を引き起こす → 活性酸素(ROS)が増える
- ROSがテロメアを直接攻撃する → テロメアがさらに短くなる
- 慢性炎症がテロメラーゼ活性を抑制する → テロメアを伸ばせなくなる
- 幹細胞のテロメアが短くなる → 組織の再生能力が低下する
- → 最初に戻る(悪循環ループ)
テロメアの長さは「生物学的な老化時計」とも言われ、心疾患・認知症・がん・免疫低下など多くの老化性疾患のリスクと関連しています。テロメアを守ることは、老化の根本的な予防につながります。
テロメアを守るために
テロメア短縮を加速させる主な要因は、慢性的なストレス・喫煙・過度な飲酒・睡眠不足・肥満・慢性炎症・酸化ストレスです。逆に、適度な運動・地中海食・良質な睡眠・ストレス管理がテロメア長の維持に有効であることが示されています。NAD⁺補充やエクソソーム療法による酸化ストレス・慢性炎症の抑制も、テロメア保護に寄与することが期待されます。
🔬 背景にある分子機序(医師向け)
患者説明の科学的根拠となる分子機序の解説です。診療の自信と説得力を高めるための情報としてご活用ください。CyTIX Academyの動画コンテンツと合わせてご参照いただくと理解が深まります。
テロメア短縮ループの分子機序
テロメア短縮・機能不全は細胞老化・DNA損傷応答・慢性炎症と双方向の悪循環を形成します。テロメアのDNA損傷は通常のDNA損傷と異なり「修復不能」であり、持続的なDDRシグナルを生じさせる点が重要です。このループは以下の連鎖で形成されます。
① テロメア短縮の機序:末端複製問題とROSによる損傷
細胞分裂ごとにDNAポリメラーゼの末端複製問題により50〜200bpのテロメア配列が失われます(複製的テロメア短縮)。テロメア配列(TTAGGG反復)はグアニン豊富であり、酸化的DNA損傷に対して特に脆弱です。8-OHdGなどの酸化損傷はシェルテリン複合体(TRF1・TRF2・POT1・TIN2・TPP1・RAP1)の機能を障害し、テロメアを非分裂細胞においても機能不全状態(telomere dysfunction without shortening)にします。テロメアDNA損傷は通常のDSBと異なりNHEJ・HRによる修復が不完全であり、持続的なDDR活性化(53BP1・γH2AX フォーカスの長期残存)を引き起こします。
② 臨界短縮テロメア → DDR → 細胞老化(#10と連動)
テロメアが臨界長(ヒトでは約5kb以下)に達するとATM/ATRキナーゼが活性化され、p53-p21-Rb経路による不可逆的な細胞周期停止が確立されます。テロメアのDNA損傷応答は二本鎖切断のDDRと同一の分子シグナルを活性化しますが、修復されないため慢性的なDDRシグナルが維持されます。老化細胞のSASPはIL-6・IL-8・TNF-αを介して慢性炎症を誘導し、慢性炎症→テロメラーゼ活性抑制→テロメア短縮加速という悪循環を形成します。
③ 慢性炎症 → テロメラーゼ抑制 → テロメア短縮加速(悪循環)
炎症性サイトカイン(IL-6・TNF-α等)の上昇はテロメラーゼ(TERT)の活性を抑制し、テロメアの維持・伸長能力を低下させます。NF-κBによるTERT転写抑制が確認されており、慢性炎症→テロメラーゼ低下→テロメア短縮加速→細胞老化増加→さらなる慢性炎症という自己増幅ループが形成されます。免疫細胞(特にT細胞・NK細胞)のテロメア短縮は免疫老化(immunosenescence)を加速させ、感染症・がんへの抵抗力を低下させます。
④ テロメア-ミトコンドリア-老化軸(#05と連動)
テロメア機能不全はp53を活性化し、p53はPGC-1α・PGC-1βの転写を抑制します(p53/PGC-1軸)。PGC-1抑制はミトコンドリア生合成の低下・ROS産生増加を招き、ROSがさらにテロメアを酸化損傷するという「テロメア-ミトコンドリア悪循環」を形成します。テロメラーゼ(TERT)はミトコンドリアに局在し、mtDNAの保護・ミトコンドリア膜電位の維持にも寄与することが示されており、テロメア短縮はミトコンドリア機能低下とも直接連動しています。
⑤ 幹細胞テロメア短縮 → 組織再生能力の低下(#15幹細胞枯渇ループと連動)
造血幹細胞・腸管上皮幹細胞・皮膚幹細胞などの組織幹細胞は高い増殖能を持つためテロメア短縮が加速しやすく、幹細胞プールの枯渇(#15と連動)・組織の再生能力低下を招きます。特発性肺線維症・骨髄不全・肝硬変などの「テロメア病」はテロメア短縮が主因の疾患であり、テロメア長の臨床的モニタリングの重要性を示しています。末梢血白血球テロメア長(LTL)は老化・疾患リスクの予測バイオマーカーとして活用できます。
引用論文
- Schellnegger M, et al. Unlocking longevity: the role of telomeres and its targeting interventions. Front Aging. 2024. PubMed
- Rossiello F, et al. Telomere dysfunction in ageing and age-related diseases. Nat Cell Biol. 2022. Nature
- Armanios M. Telomeres and age-related disease: how telomere biology informs clinical paradigms. J Clin Invest. 2013. PubMed
- NRF2 signaling pathway and telomere length in aging and age-related diseases. Mol Cell Biochem. 2023. Springer
- Wagner N, Wagner KD. Controversies and Recent Advances in Senescence and Aging. Cells. 2023. PubMed
CyTIXのアプローチ
テロメア短縮ループへの介入は、酸化ストレス・慢性炎症の抑制とNAD⁺補充の組み合わせが最も合理的なアプローチです。
NAD⁺ナドプラ®療法(NMN点滴・NAD⁺点滴・サプリ・点鼻セットなど、NAD⁺を補填・管理する複数の手段を統合した療法)は、テロメア短縮を加速させる酸化ストレス(ROS)とミトコンドリア機能低下に直接アプローチします。SIRT1・SIRT6の活性回復はDNA修復効率を高め、シェルテリン複合体の機能維持に寄与します。またSIRT1によるNF-κB抑制はテロメラーゼ活性を保護し、テロメア短縮加速の悪循環を断ち切る効果が期待されます。
WJ幹細胞エクソソーム療法は、テロメア短縮による慢性炎症・組織障害を抑制し、幹細胞の機能維持をサポートすることでテロメア短縮ループの増幅を断ち切るアプローチとして期待されています。
▶ 完全ガイドを見る