🧑💼 お客様への伝え方
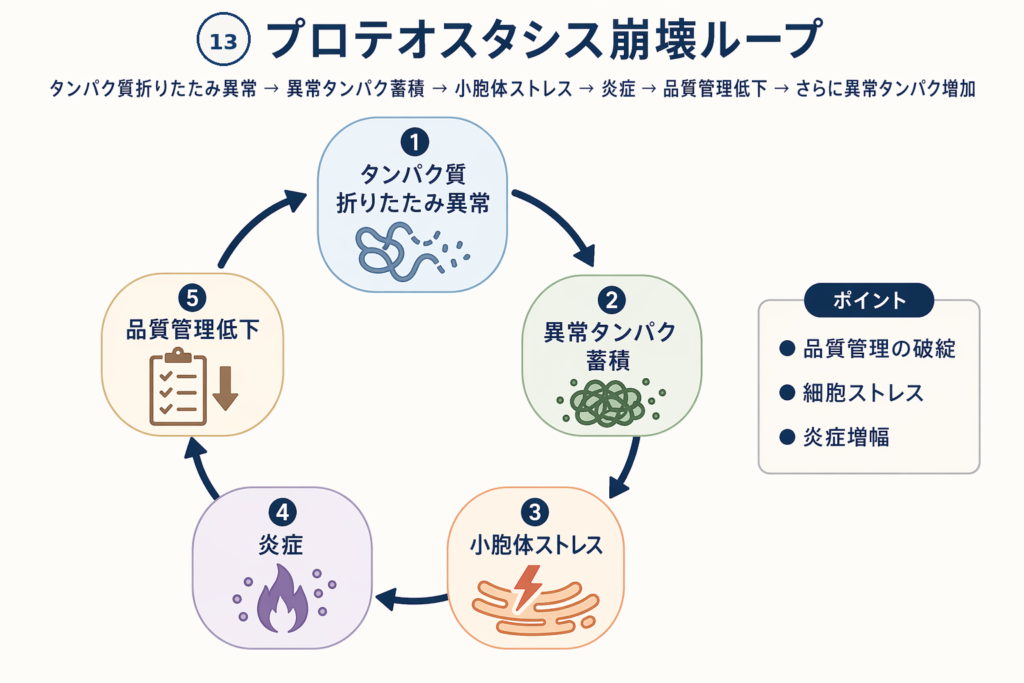
ロンジェビティ医療は「病気になる前」の健康な方を対象とした予防医療です。このセクションは、外来でお客様にこのループをわかりやすく伝えるための言葉の例です。専門用語を避け、日常のイメージで伝えることを意識しています。そのままお使いいただくか、先生ご自身の言葉にアレンジしてご活用ください。
細胞には「タンパク質の品質管理システム」がある
私たちの体の中では、毎秒数百万個ものタンパク質が作られています。タンパク質は正しく折りたたまれた形(立体構造)であって初めて機能します。しかし合成の際にエラーが起きたり、酸化ストレス・熱などで変性したりすると、「異常タンパク質(ミスフォールドタンパク質)」が生じます。
健康な細胞には、この異常タンパク質を検出・修復・除去する「プロテオスタシス(タンパク質恒常性)ネットワーク」が備わっています。分子シャペロン(HSP70・HSP90など)が異常タンパク質を正しい形に折り直し、それでも修復できない場合はユビキチンプロテアソームシステム(UPS)やオートファジーが分解・除去します。
しかし加齢とともにこのシステムが劣化し始めます:
- シャペロン機能が低下する → 異常タンパク質が蓄積し始める
- UPS・オートファジーが低下する → 異常タンパク質が除去されない
- 異常タンパク質が凝集する → 細胞毒性が生じる
- 細胞毒性がミトコンドリアを障害する → ROSが増加する
- ROSがさらにタンパク質を変性させる → 異常タンパク質がさらに増える
- 慢性炎症が起きる → プロテオスタシスネットワークがさらに障害される
- → 最初に戻る(悪循環ループ)
この「プロテオスタシス崩壊ループ」は、アルツハイマー病(アミロイドβ・タウ)・パーキンソン病(α-シヌクレイン)・筋萎縮性側索硬化症(TDP-43)など多くの神経変性疾患の根本に関わっています。また白内障・心筋症・肝疾患にも深く関連しています。
プロテオスタシスを守るために
プロテオスタシスを維持するためには、酸化ストレスの抑制(#02と連動)、オートファジーの活性化(#11と連動)、そして熱ショック応答を刺激する適度な運動・温熱療法が有効です。NAD⁺補充によるサーチュイン活性化もシャペロン発現を促進し、プロテオスタシスの維持に寄与することが示されています。
🔬 背景にある分子機序(医師向け)
患者説明の科学的根拠となる分子機序の解説です。診療の自信と説得力を高めるための情報としてご活用ください。CyTIX Academyの動画コンテンツと合わせてご参照いただくと理解が深まります。
プロテオスタシス崩壊ループの分子機序
プロテオスタシス(タンパク質恒常性)ネットワークは、分子シャペロン・UPS・オートファジーリソソーム経路(ALP)・小胞体ストレス応答(UPR)・ミトコンドリアUPR(UPRmt)から構成されます。加齢に伴うプロテオスタシスの崩壊は、ミトコンドリア機能低下・オートファジー低下・慢性炎症・細胞老化と多重の悪循環を形成します。このループは以下の連鎖で形成されます。
① 熱ショック応答(HSR)の加齢性低下 → シャペロン機能不全
HSF1(熱ショック転写因子1)は主要なシャペロン(HSP70・HSP90・HSP27・HSP40等)の転写を制御します。加齢に伴いHSF1の活性化能力が低下し、プロテオトキシックストレスに対するシャペロン発現応答が減弱します。SIRT1はHSF1の脱アセチル化・活性化を介してシャペロン発現を促進しますが、NAD⁺枯渇(#06と連動)によるSIRT1低下はこの経路を障害します。シャペロン機能の低下により、ミスフォールドタンパク質の再折りたたみ・凝集予防・プロテアソームへの誘導が障害されます。
② UPS機能低下 → 異常タンパク質蓄積
加齢に伴い26Sプロテアソームの活性(特に20Sコアの触媒活性)が低下します。酸化ストレスによるプロテアソームサブユニットの酸化修飾・架橋形成がプロテアソーム機能を直接障害します。ポリユビキチン化タンパク質の蓄積はプロテアソームを閉塞させ(プロテアソーム詰まり)、UPS全体のスループットをさらに低下させます。タンパク質凝集体はUPSとオートファジーの双方を障害し(クロスインヒビション)、プロテオスタシス崩壊が自己増幅します。
③ 小胞体ストレス応答(UPR)の慢性化 → 炎症・アポトーシス
小胞体(ER)内でのミスフォールドタンパク質蓄積はERストレスを誘発し、IRE1α・PERK・ATF6の三経路からなるUPRが活性化されます。急性UPRはプロテオスタシス回復に寄与しますが、慢性的なUPR活性化はNF-κBを介した炎症誘導・CHOP/GADD153を介したアポトーシス促進に転じます。加齢に伴うERストレスの慢性化は、インスリン抵抗性(#03と連動)・アテローム硬化・神経変性の病態進行に寄与します。
④ ミトコンドリアUPR(UPRmt)と「ミトコンドリア-プロテオスタシス悪循環」(#05と連動)
ミトコンドリア内のミスフォールドタンパク質はClpP・LONP1などのミトコンドリアプロテアーゼとHsp60・mtHsp70などのシャペロンによって処理されます。加齢・ROS増加によりミトコンドリアタンパク質の変性が蓄積すると、UPRmtが活性化されます。UPRmt活性化はNAD⁺/SIRT1シグナルと連動しており、ミトコンドリア機能低下→UPRmt過剰活性化→ミトコンドリアタンパク質品質管理の失敗→さらなるミトコンドリア機能低下という悪循環を形成します。異常タンパク質の蓄積はETCを直接障害し、ROS産生を増加させます(#05と連動)。
⑤ 神経変性疾患との連動:プリオン様伝播
アミロイドβ・タウ・α-シヌクレイン・TDP-43などの病的タンパク質凝集体は、細胞間をエクソソーム・直接接触を介してプリオン様に伝播し、プロテオスタシス崩壊を隣接細胞に波及させます。これらの凝集体はUPS・オートファジーの双方を阻害し(#11と連動)、神経細胞のプロテオスタシス崩壊を自己増幅させます。SIRT1の活性回復はα-シヌクレインの凝集抑制・タウの脱アセチル化促進・アミロイドβクリアランス改善に寄与することが示されています。
引用論文
- Loss of Proteostasis. Lifespan Research Institute. 2025.
- Proteostasis and neurodegeneration: a closer look at autophagy in Alzheimer’s disease. Front Aging Neurosci. 2023. Frontiers
- Klaips CL, et al. Build-UPS and break-downs: metabolism impacts on proteostasis and aging. Cell Death Differ. 2020. Nature
- Crosstalk Between Chaperone-Mediated Protein Disaggregation and Proteolytic Pathways in Aging and Disease. Front Mol Biosci. 2019. PubMed
- Kaushik S, Cuervo AM. Loss of hepatic chaperone-mediated autophagy accelerates proteostasis failure in aging. Aging Cell. 2015. PubMed
CyTIXのアプローチ
プロテオスタシス崩壊ループへの介入は、NAD⁺/SIRT1/HSF1軸の回復とオートファジー活性化の組み合わせが最も合理的なアプローチです。
NAD⁺ナドプラ®療法(NMN点滴・NAD⁺点滴・サプリ・点鼻セットなど、NAD⁺を補填・管理する複数の手段を統合した療法)は、SIRT1活性の回復を通じてHSF1を活性化し、シャペロン発現を促進することでプロテオスタシスの維持に寄与します。また酸化ストレスの根本にあるミトコンドリア機能低下・NAD⁺枯渇への直接介入により、タンパク質変性の主要な原因を抑制します。
WJ幹細胞エクソソーム療法は、慢性炎症の抑制とUPR正常化を通じてプロテオスタシス崩壊ループの増幅を断ち切るアプローチとして期待されています。
▶ 完全ガイドを見る