患者さんへの説明
細胞には「自己掃除機能」がある
私たちの細胞の中では、毎日古くなったタンパク質・壊れたミトコンドリア・不要な細胞内成分が蓄積しています。これらを分解・リサイクルする細胞の「自己掃除機能」を「オートファジー(自食作用)」と呼びます。
オートファジーは体の健康維持に不可欠な仕組みです。大隅良典博士がこの仕組みを解明し、2016年にノーベル生理学・医学賞を受賞したことで広く知られるようになりました。酵母・線虫・ハエ・マウスのすべての生物で「オートファジーを活性化すると寿命が延びる」ことが示されており、ロンジェビティ医療における重要な介入ターゲットです。
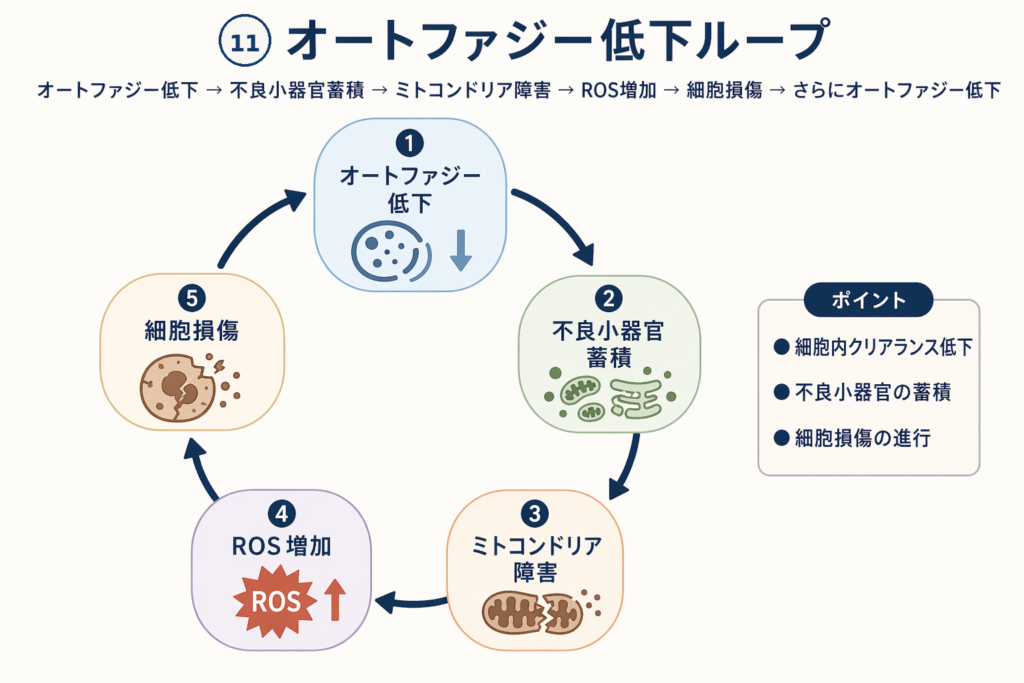
しかし加齢とともにこのオートファジー機能が低下します。すると細胞内にゴミ(異常タンパク質・壊れたミトコンドリア)が蓄積し始め、悪循環が始まります:
- オートファジーが低下する → 壊れたミトコンドリアが除去されない
- 機能不全ミトコンドリアが蓄積する → 活性酸素(ROS)が増える
- ROSが増える → オートファジー機構自体が損傷される
- 異常タンパク質が蓄積する → 細胞老化・炎症が促進される
- 慢性炎症が起きる → オートファジーがさらに抑制される
- mTORが過活性化される → オートファジー開始シグナルが遮断される
- → 最初に戻る(悪循環ループ)
オートファジーの低下は、アルツハイマー病(アミロイドβ・タウの蓄積)・パーキンソン病(α-シヌクレインの蓄積)・心疾患・がんなど多くの老化性疾患の根本に関わっています。「細胞のお掃除」を維持することが、老化予防の重要な柱のひとつです。
オートファジーを活性化するには
オートファジーはすべての主要な長寿介入(カロリー制限・断食・運動)に共通して活性化されることが示されています。食後に一定の空腹時間を設ける(間欠的断食)、定期的な有酸素運動を行うことが、オートファジーを自然に高める実践的な方法です。医療的介入としてはラパマイシン(mTOR阻害)・スペルミジン・NAD⁺補充などが研究されています。
医師向け:機序の詳細
オートファジー低下ループの分子機序
オートファジー(マクロオートファジー)は40以上のATG(オートファジー関連)タンパク質によって制御される多段階の細胞リサイクル過程であり、組織特異的な発現パターンと文脈依存的な制御を持ちます。加齢に伴うオートファジー低下は、上流の栄養センシング経路(mTORC1・AMPK)の異常・リソソーム機能の低下・オートファジー関連タンパク質の発現低下などの複合的な結果です。このループは以下の連鎖で形成されます。
① mTORC1過活性化 → オートファジー開始の遮断
mTORC1(mechanistic Target of Rapamycin Complex 1)はオートファジーの主要な抑制因子です。加齢・インスリン抵抗性・慢性炎症によりmTORC1が過活性化されると、ULK1(オートファジー開始キナーゼ)のリン酸化・不活性化を介してオートファジー誘導が遮断されます。AMPKはエネルギー不足のセンサーとしてmTORC1を抑制しULK1を活性化しますが、加齢に伴うAMPK活性の低下がこのバランスを崩します。NAD⁺/SIRT1シグナルはAMPKを活性化してmTORC1を抑制する経路を介してオートファジーを促進しており、NAD⁺枯渇(#06と連動)はこの経路を障害します。
② マイトファジー(選択的オートファジー)の低下 → 機能不全ミトコンドリアの蓄積
マイトファジー(ミトコンドリア選択的オートファジー)はPINK1/Parkinユビキチン依存経路とBNIP3/FUNDC1受容体依存経路により制御されます。加齢に伴うマイトファジー効率の低下は、機能不全ミトコンドリアの蓄積→ROS産生増加→mtDNA損傷→マイトファジー機構自体の損傷という「ミトコンドリア損傷-ROS-老化ダメージ」の悪循環を形成します(#05と連動)。老化細胞における脂質ドロップレット蓄積はp62依存的にマイトファジーを阻害し、ミトコンドリア機能低下を加速させます。
③ プロテオスタシス崩壊 → 異常タンパク質蓄積 → 細胞老化(#09プロテオスタシス崩壊ループと連動)
オートファジーリソソーム経路(ALP)とユビキチンプロテアソーム経路(UPS)は協調してプロテオスタシスを維持します。加齢に伴うオートファジー低下により、異常タンパク質凝集体(p62・ユビキチン化タンパク質・アミロイドβ・α-シヌクレイン・タウ等)が蓄積します。慢性ストレス(細胞老化誘発因子)下では分解容量が分解要求量を下回り、「異常タンパク質蓄積→さらなるストレス→プロテオスタシス崩壊→細胞老化」という悪循環を形成します。
④ オートファジー低下 → SASP増幅 → 細胞老化ループとの連動(#10と連動)
オートファジーは通常、老化細胞が分泌するSASP構成要素の一部を分解・制御する機能を持ちます。オートファジー低下によりSASPの産生・分泌が増幅され、慢性炎症がさらにオートファジーを抑制するという悪循環が形成されます。またcGAS-STINGシグナルは通常オートファジーにより制御されますが、オートファジー低下によりcGASが細胞質クロマチンを認識し続け、インターフェロン応答→NF-κB→SASP増幅のループが維持されます。
⑤ オートファジーの二面性:がん抑制 vs がん促進
オートファジーは腫瘍形成の初期段階では腫瘍抑制的(前がん細胞の除去・ゲノム安定性の維持)に機能しますが、進行がんでは腫瘍促進的(低酸素・栄養枯渇環境での生存支援)に機能します。加齢に伴うオートファジー低下は初期腫瘍形成リスクを高める一方、過剰なオートファジー活性化も病的プロセスを加速させる「諸刃の剣」であり、治療的介入の最適化が重要です。
引用論文
- Lim SHY, et al. Molecular Mechanisms of Autophagy Decline during Aging. Cells. 2024. PubMed
- Targeting mitochondrial autophagy for anti-aging. Cell Death Discov. 2025. PubMed
- Hamazaki J, Murata S. Relationships between protein degradation, cellular senescence, and organismal aging. J Biochem. 2024. PubMed
- Autophagy at the intersection of aging, senescence, and cancer. Aging Cell. 2022. PubMed
- Nakamura S, Yoshimori T. Agephagy – Adapting Autophagy for Health During Aging. Cells. 2019. PubMed
CyTIXのアプローチ
オートファジー低下ループへの介入は、NAD⁺/SIRT1/AMPK軸の回復が最も直接的なアプローチです。
NAD⁺ナドプラ®療法(NMN点滴・NAD⁺点滴・サプリ・点鼻セットなど、NAD⁺を補填・管理する複数の手段を統合した療法)は、NAD⁺/SIRT1シグナルの回復を通じてAMPKを活性化し、mTORC1を適切に抑制することでオートファジー活性の回復を目指します。SIRT1によるFOXO転写因子の脱アセチル化はオートファジー関連遺伝子(LC3・Beclin1・ATG等)の発現を促進し、マイトファジー機能の回復にも寄与します。
またWJ幹細胞エクソソーム療法は、オートファジー低下による組織障害を修復し、慢性炎症を抑制することでオートファジー低下ループの増幅を断ち切るアプローチとして期待されています。