患者さんへの説明
老化した細胞は死なずに「毒」を出し続ける
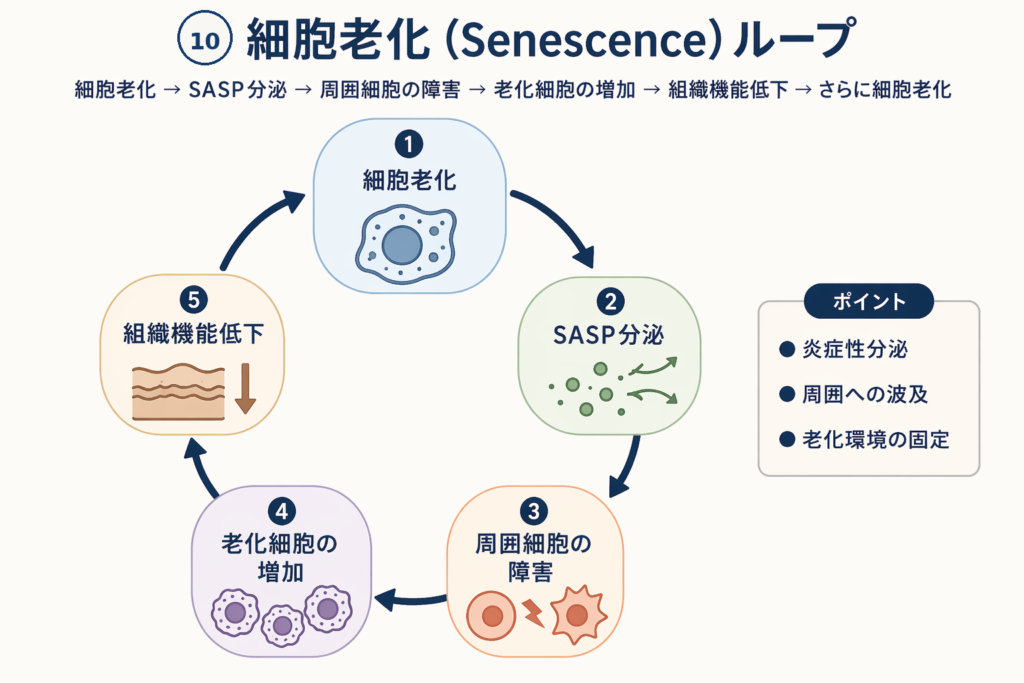
体の細胞は、傷ついたり限界まで分裂したりすると、「もうこれ以上増殖してはいけない」という指令を受けて活動を停止します。これが「細胞老化(Senescence)」という状態です。
細胞老化は本来、傷ついた細胞ががん化するのを防ぐための、体の賢い防衛機構です。若い頃は、老化した細胞を免疫システムがきちんと除去してくれます。
しかし問題は加齢とともに起きます。老化細胞の蓄積スピードが、免疫による除去スピードを上回ると、老化細胞が体内に居座り続けます。そしてこの老化細胞は死なずに、周囲に炎症を引き起こす物質(SASP)を分泌し続けます:
- DNA損傷・酸化ストレスが増える → 細胞老化が誘導される
- 老化細胞がSASPを分泌する → 周囲に慢性炎症が広がる
- SASPが正常な隣の細胞にも老化を誘導する → 老化細胞がさらに増える
- 慢性炎症が免疫細胞を老化させる → 老化細胞を除去できなくなる
- 老化細胞が蓄積する → 組織・臓器の機能が低下する
- 臓器機能低下がDNA損傷・酸化ストレスを増やす → さらに細胞老化が誘導される
- → 最初に戻る(悪循環ループ)
老化細胞を若いマウスに移植すると体の機能が低下し、老齢マウスに移植するとさらに老化が加速・死亡リスクが高まることが示されています。逆に老化細胞を除去(セノリシス)すると、多くの老化性疾患が改善することも確認されています。老化細胞の制御が、ロンジェビティ医療の重要な標的のひとつです。
SASPとは何か
SASP(老化関連分泌表現型)とは、老化細胞が分泌する炎症性サイトカイン・成長因子・タンパク質分解酵素などの混合物です。傷の修復や免疫調節に一時的には役立ちますが、慢性的に分泌され続けると周囲の組織に炎症・線維化・機能低下をもたらします。
医師向け:機序の詳細
細胞老化ループの分子機序
細胞老化(Cellular Senescence)は不可逆的な細胞周期停止を特徴とし、SASP・慢性炎症・免疫老化と双方向の悪循環を形成します。SASPは機能的二面性を持ち(短期的:組織修復・腫瘍抑制、長期的:慢性炎症・線維化・腫瘍促進)、この二面性がロンジェビティ医療における治療標的の複雑さを生んでいます。このループは以下の連鎖で形成されます。
① 細胞老化の誘導因子と経路
細胞老化の主要な誘導因子は、テロメア短縮(複製老化)・DNA二本鎖切断(DNA損傷誘発老化)・酸化ストレス・ミトコンドリア機能不全(MiDAS)・癌遺伝子活性化(OIS)です。分子経路はp53-p21-Rb経路(DNA損傷応答依存性)とp16INK4a-Rb経路(エピゲノム変化依存性)の二系統があり、いずれも不可逆的な細胞周期停止を確立します。老化細胞はアポトーシス抵抗性を獲得(BCL-2・BCL-XL過剰発現)しながら代謝活性を維持し、SASPを持続的に分泌します。
② SASP → 傍分泌性老化伝播(Paracrine Senescence)
SASPの主要構成要素(IL-6・IL-8・TNF-α・MMP-3・MMP-9・GROα・VEGF等)は傍分泌・内分泌的に作用し、隣接する正常細胞にDDR(DNA損傷応答)を活性化して老化を誘導します(傍分泌性老化伝播)。また細胞質クロマチン断片(CCF)がcGAS-STINGシグナルを活性化し、I型インターフェロン応答→NF-κB活性化→SASPの増幅という二次的ループを形成します。SASPはNF-κB・C/EBPβ・mTOR・p38MAPKなど複数の転写因子によって制御され、細胞種・組織文脈・時間的動態により組成が変動します。
③ 慢性炎症 → 免疫老化 → 老化細胞蓄積の悪循環
SASPによる慢性炎症はNK細胞・マクロファージ・T細胞などの免疫細胞を老化させ(免疫老化:immunosenescence)、老化細胞の認識・除去能力を低下させます。免疫老化により老化細胞のクリアランスが障害されると、老化細胞が組織に蓄積し、SASPによる炎症がさらに増幅されます。骨髄・肝臓・肺などの臓器での持続的炎症は、臓器機能障害→酸化ストレス増加→新たな細胞老化誘導という三重の悪循環を形成します。
④ 多臓器への影響:心血管・神経・筋骨格系
心筋細胞・血管内皮細胞の老化は心臓リモデリング・動脈硬化を促進します。グリア細胞(アストロサイト・ミクログリア)の老化は神経炎症を誘導し、アルツハイマー病・パーキンソン病の病態進行に寄与します(#19神経変性ループと連動)。軟骨細胞・骨芽細胞の老化は関節軟骨の分解・骨密度低下をもたらします(#20筋肉減少ループと連動)。腎臓においては、老化細胞と炎症の悪循環が糸球体硬化・腎線維化を促進します。
⑤ セノリシス・セノモルフィクスの治療戦略
セノリシス(老化細胞の選択的除去):Navitoclax(BCL-2/BCL-XL阻害)・Dasatinib+Quercetin(D+Q)・Fisetin等が前臨床・臨床研究で検討されています。セノモルフィクス(SASPの調節):ラパマイシン(mTOR阻害)・JAK阻害剤・NAD⁺補充(SASP構成要素の抑制)等が研究されています。NAD⁺/SIRT1軸の回復はNF-κB抑制を介してSASPを調節し、セノモルフィクスとして機能します(#06と連動)。WJ幹細胞エクソソームは免疫調節・抗炎症作用を介してSASPを抑制する可能性が示されています。
引用論文
- Liu Y, et al. Inflammation and aging: signaling pathways and intervention therapies. Signal Transduct Target Ther. 2023. Nature
- SASP Modulation for Cellular Rejuvenation and Tissue Homeostasis. PMC. 2025. PubMed
- Saliev T, Singh PB. Targeting Senescence: A Review of Senolytics and Senomorphics in Anti-Aging Interventions. Biomolecules. 2025. PubMed
- Targeting Cellular Senescence: Pathophysiology in Multisystem Age-Related Diseases. PMC. 2025. PubMed
- Recent Advances in Aging and Immunosenescence: Mechanisms and Therapeutic Strategies. PMC. 2025. PubMed
- From Senescent Cells to Systemic Inflammation: The Role of Inflammaging in Age-Related Diseases and Kidney Dysfunction. Cells. 2025. MDPI
CyTIXのアプローチ
細胞老化ループへの介入は、SASP抑制と組織修復の両面からのアプローチが最も合理的です。
NAD⁺ナドプラ®療法(NMN点滴・NAD⁺点滴・サプリ・点鼻セットなど、NAD⁺を補填・管理する複数の手段を統合した療法)は、SIRT1活性の回復を通じてNF-κBシグナルを抑制し、SASPの構成要素を調節するセノモルフィクスとして機能します。またSIRT1/SIRT6の活性回復はDNA修復効率を高め、新たな細胞老化の誘導を抑制します。
WJ幹細胞エクソソーム療法は、老化細胞が引き起こす慢性炎症を抑制し、SASP由来の組織障害を修復する免疫調節・抗炎症作用が期待されます。老化細胞の蓄積によって傷ついた組織の再生を促進することで、細胞老化ループの増幅を断ち切るアプローチとして位置づけられています。