患者さんへの説明
DNAは毎日傷つき、そして修復されている
私たちの体の設計図であるDNAは、毎日何万もの傷(損傷)を受けています。紫外線・活性酸素・化学物質・複製エラーなど、原因はさまざまです。しかし若い頃は、細胞が持つ「DNA修復システム」がこれらの傷を素早く修復してくれます。
問題は加齢とともにこの修復能力が低下することです。修復しきれないDNAの傷が蓄積し始めると、細胞は「これ以上増殖してはいけない」という判断を下します。これが「細胞老化(Senescence)」という状態です。
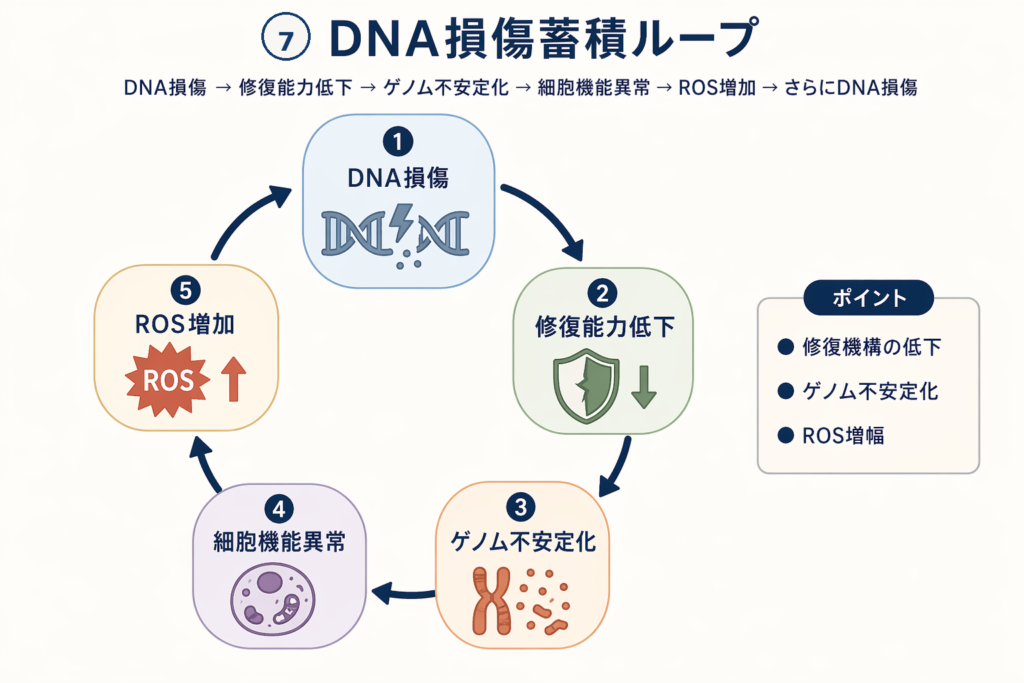
細胞老化した細胞は死ぬわけではなく、体内に居座り続け、周囲の細胞に悪影響を与える物質を分泌し続けます。これが「DNA損傷蓄積ループ」の始まりです:
- DNA損傷が蓄積する → 細胞老化(Senescence)が起きる
- 老化細胞がSASPを分泌する → 周囲に慢性炎症が広がる
- 慢性炎症が活性酸素を増やす → さらにDNAが傷つく
- DNA修復にNAD⁺が消費される → NAD⁺が枯渇する
- NAD⁺枯渇でDNA修復能力がさらに低下する → 損傷がさらに蓄積する
- 老化細胞がさらに増える → 組織・臓器の機能が低下する
- → 最初に戻る(悪循環ループ)
このループが全身で起きることで、がん・認知症・心疾患・免疫低下など、多くの老化性疾患のリスクが高まります。DNA損傷を減らし、修復能力を高めることが、老化予防の根本的なアプローチです。
日常生活でできるDNA保護
DNA損傷を最小化するために重要なのは、活性酸素を増やさないこと(過度な飲酒・喫煙・紫外線・過食を避ける)と、DNA修復に必要なNAD⁺を補充することです。また十分な睡眠はDNA修復が最も活発に行われる時間帯であり、睡眠の質の向上もDNA保護に直結します。
医師向け:機序の詳細
DNA損傷蓄積ループの分子機序
DNA損傷の蓄積は老化の最も根本的なホールマークのひとつです。ゲノム不安定性・細胞老化・慢性炎症・NAD⁺枯渇と双方向の悪循環を形成します。このループは以下の連鎖で形成されます。
① DNA損傷の原因と蓄積機序
内因性DNA損傷の主要な原因は、ミトコンドリア由来の活性酸素(ROS)による酸化的DNA損傷(8-OHdG・一本鎖切断・二本鎖切断)、DNA複製エラー、自発的脱塩基・脱アミノ化などです。加齢に伴いDNA修復経路(BER・NER・NHEJ・HR)の効率が低下し、損傷の蓄積が加速します。老化細胞のトランスクリプトーム解析では、NER・BER・NHEJ・HRを含む必須DNA修復遺伝子群が広範に抑制されていることが確認されており、老化細胞が「時限爆弾」として機能する可能性が示されています。
② DNA損傷応答(DDR)→ 細胞老化(Senescence)
DNA二本鎖切断はATM・ATRキナーゼを活性化し、MDC1・BRCA1・53BP1などのDDRタンパク質が動員されます。修復不能な損傷が持続すると、p53リン酸化を介したp21の転写活性化により細胞周期が不可逆的に停止します(p53-p21-Rb経路)。またエピゲノム変化を介したp16INK4a-Rb経路も細胞老化を確立します。老化細胞はアポトーシス抵抗性を獲得しながら代謝活性を維持し、SASPを分泌し続けます。
③ SASP → 慢性炎症・周囲細胞への老化伝播(悪循環)
SASP(老化関連分泌表現型)にはIL-6・IL-8・TNF-α・MMP・増殖因子などが含まれます。SASPは傍分泌・内分泌的に作用し、周囲の正常細胞に老化を誘導します(老化の伝播)。また細胞質クロマチン断片(cytoplasmic chromatin)がcGAS-STINGシグナルを活性化し、インターフェロン応答を介した慢性炎症を促進します。組織特異的なDNA修復欠損(ERCC1欠損モデル)でも非標的組織での老化細胞増加が観察されており、cell non-autonomous mechanismによる老化の全身伝播が示されています。
④ DNA損傷 → PARP1活性化 → NAD⁺枯渇(#06と連動)
DNA損傷センサーとしてのPARP1はDNA一本鎖切断を認識し、PAR(ポリADPリボース)鎖の合成によりNAD⁺を大量消費します。NAD⁺枯渇→SIRT1/SIRT6低下→DNA修復効率低下→DNA損傷蓄積という自触媒的な悪循環が形成されます(#06 NAD⁺枯渇ループと連動)。ATM活性化とNAD⁺/SIRT1/PARP1軸はDNAメチル化時計(エピゲノム時計)と連動し、生物学的年齢の加速に寄与します。
⑤ ゲノム不安定性 → 幹細胞枯渇・がん化
DNA損傷が修復不能なレベルに達した高度損傷細胞はアポトーシスへ誘導されます。これはがん化を防ぐ保護機構ですが、同時に幹細胞プールを枯渇させ(#15幹細胞枯渇ループと連動)、組織の再生能力を低下させます。一方、DNA修復が不正確(error-prone)に行われると変異が蓄積し、がん化リスクが高まります。DNA損傷の蓄積は、老化とがんという一見逆の方向に同時に作用する二面的なリスクを持ちます。
引用論文
- Hoeijmakers JHJ, et al. Targeting DNA damage in ageing: towards supercharging DNA repair. Nat Rev Drug Discov. 2025. Nature
- The Converging Roles of Nucleases and Helicases in Genome Maintenance and the Aging Process. PMC. 2025. PubMed
- Broad repression of DNA repair genes in senescent cells identified by integration of transcriptomic data. PMC. 2025. PubMed
- Cellular Senescence in Aging, Tissue Repair and Regeneration. PMC. 2022. PubMed
- Schumacher B, et al. DNA damage responses in ageing. Open Biol. 2021. PubMed
CyTIXのアプローチ
DNA損傷蓄積ループへの介入は、NAD⁺補充とエクソソーム療法の組み合わせが最も合理的なアプローチです。
NAD⁺ナドプラ®療法(NMN点滴・NAD⁺点滴・サプリ・点鼻セットなど、NAD⁺を補填・管理する複数の手段を統合した療法)は、DNA修復の核心にあるNAD⁺/PARP1/SIRT1軸を直接補充することで、DNA修復能力の回復・老化細胞の蓄積抑制・慢性炎症の軽減を目指します。SIRT1・SIRT6の活性回復はDNA損傷の修復効率を高め、ゲノム安定性の維持に寄与します。
またWJ幹細胞エクソソーム療法は、SASP由来の慢性炎症を抑制し、DNA損傷による組織障害の修復をサポートします。老化細胞の除去(セノリシス)と組織再生の促進により、DNA損傷蓄積ループの増幅を断ち切るアプローチとして期待されています。