患者さんへの説明
NAD⁺とは何か——老化を左右する「司令塔」
NAD⁺(ニコチンアミドアデニンジヌクレオチド)という言葉を聞いたことはありますか?近年、長寿研究の世界で最も注目されている分子のひとつです。
NAD⁺は体のすべての細胞に存在し、エネルギーの産生・DNA修復・遺伝子の制御・免疫機能など、生命活動の根幹を担う「司令塔」のような役割を果たしています。しかしこのNAD⁺は、加齢とともに急激に減少します。20代と比較すると、50代では約半分にまで低下することが知られています。
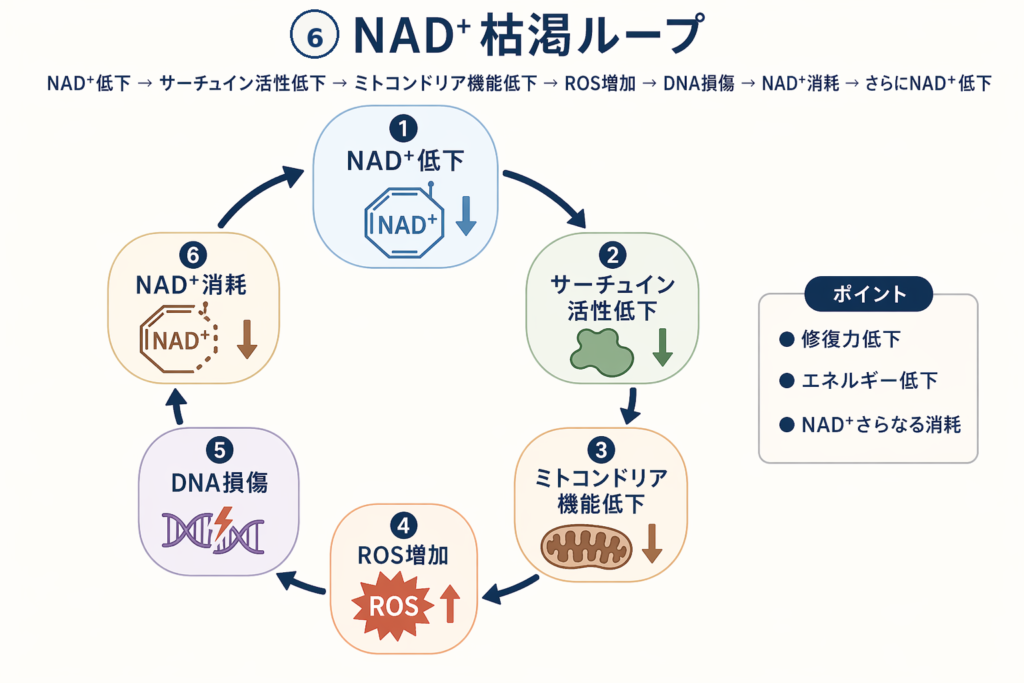
NAD⁺が減ると、体の至る所で機能不全が起き、しかもそれが悪循環を作り出します:
- NAD⁺が減る → ミトコンドリアのエネルギー産生が低下する
- DNA損傷が増える → 修復のためNAD⁺がさらに消費される
- NAD⁺が枯渇する → 長寿遺伝子(サーチュイン)が働けなくなる
- サーチュインが低下する → DNA損傷がさらに蓄積する
- 慢性炎症が起きる → 炎症応答でもNAD⁺が消費される
- → 最初に戻る(悪循環ループ)
この「NAD⁺枯渇ループ」は、慢性疲労・筋力低下・認知機能低下・免疫低下・代謝障害など、老化のあらゆる側面と関連しています。NAD⁺を補充することは、老化の悪循環を断ち切る最も直接的なアプローチのひとつです。
NMNとNAD⁺補充の意味
NMN(ニコチンアミドモノヌクレオチド)はNAD⁺の前駆体(材料)です。NMNを補充することでNAD⁺の体内レベルを高め、ミトコンドリア機能の回復・DNA修復能力の向上・長寿遺伝子の活性化を目指します。点滴による直接投与はサプリメントよりも吸収効率が高く、より確実なNAD⁺補充が期待できます。
医師向け:機序の詳細
NAD⁺枯渇ループの分子機序
NAD⁺は細胞内の酸化還元反応の中心的な補酵素であり、同時にPARP・サーチュイン・CD38・SARM1などの酵素の基質として消費されます。加齢に伴うNAD⁺枯渇は、これらの競合的消費と産生低下の複合的な結果です。このループは以下の連鎖で形成されます。
① DNA損傷蓄積 → PARP1過活性 → NAD⁺消費の悪循環
加齢に伴う慢性的なDNA損傷の蓄積により、PARP1(ポリADPリボースポリメラーゼ1)が慢性的に活性化され、NAD⁺を大量消費します。NAD⁺枯渇によりSIRT1・SIRT6の活性が低下すると、DNA損傷の修復効率がさらに低下し、PARP1の活性化が維持されます。この「NAD⁺枯渇→SIRT1低下→DNA損傷増加→PARP1活性化→さらなるNAD⁺枯渇」という自触媒的な悪循環がNAD⁺枯渇ループの核心です。老齢マウスでは肝臓・骨格筋においてPARP活性の慢性的亢進が確認されており、NMN投与によりDBC1-PARP1複合体を解離させてPARP活性を回復させることが示されています。
② CD38の加齢性増加 → NAD⁺分解亢進
CD38はNAD⁺を加水分解する主要なNAD分解酵素(NADase)です。加齢・慢性炎症に伴いCD38の発現が増加し、NMN・NRを含むNAD⁺前駆体も分解します。CD38ノックアウトマウスではNAD⁺レベルが全身的に上昇し、SIRT1活性と代謝機能の改善が確認されています。PARP1・CD38・核サーチュインはすべて同一のNAD⁺プールをめぐって競合しており、加齢に伴いこの競合が激化します。
③ SIRT1/SIRT3低下 → ミトコンドリア機能低下・エピゲノム異常
NAD⁺依存性脱アセチル化酵素であるSIRT1はPGC-1αを脱アセチル化・活性化し、ミトコンドリア生合成を促進します。SIRT3はミトコンドリア内のOXPHOS複合体・SOD2・IDH2などを脱アセチル化し、ミトコンドリア機能を維持します。NAD⁺枯渇によるSIRT1/SIRT3の活性低下は、ミトコンドリア機能低下(#05と連動)・エピゲノム異常(#09と連動)・インスリン抵抗性(#03と連動)という多重の悪循環を形成します。PGC-1αのアセチル化亢進はミトコンドリア生合成を抑制し、PARP1活性化とさらなるNAD⁺消費の悪循環を強化します。
④ NAD⁺産生低下:NAMPT活性の加齢性低下
NAD⁺のサルベージ経路における律速酵素NAMPT(ニコチンアミドホスホリボシルトランスフェラーゼ)の活性が加齢・慢性炎症により低下します。これにより、NMN→NAD⁺への変換効率が低下し、NAD⁺の産生側からも枯渇が促進されます。またde novo経路(トリプトファン→キヌレニン→NAD⁺)も加齢に伴い変動し、腸内環境悪化(#04と連動)によるキヌレニン経路の異常活性化がNAD⁺代謝に影響します。
⑤ NAD⁺/PARP1/SIRT1軸とエピゲノム時計との関連
NAD⁺/PARP1/SIRT1軸はDNAメチル化パターン(エピゲノム時計)と密接に関連しています。SIRT1・SIRT6によるヒストン脱アセチル化はクロマチン構造の維持に必須であり、NAD⁺枯渇によるサーチュイン低下はエピゲノム不安定性を招き、老化関連遺伝子の発現変化を促進します(#09エピゲノム変化ループと連動)。NAD⁺補充によるDNAメチル化時計の逆転が複数の研究で示されており、生物学的年齢の改善指標としてNAD⁺レベルのモニタリングが注目されています。
引用論文
- Guarente L. NAD+ and Sirtuins in Aging and Disease. Trends Cell Biol. 2014. PubMed
- Fang EF, et al. The NAD+/PARP1/SIRT1 Axis in Aging. Cell Metab. 2017. PubMed
- Katsyuba E, Auwerx J. NAD+ biosynthesis, aging, and disease. EMBO J. 2017. PubMed
- Luo X, Kraus WL. SIRT1/PARP1 crosstalk: connecting DNA damage and metabolism. Trends Biochem Sci. 2012. PubMed
- Mohamed JS, et al. Dysregulation of SIRT-1 in aging mice increases skeletal muscle fatigue by a PARP-1-dependent mechanism. Aging. 2014. PubMed
CyTIXのアプローチ
NAD⁺枯渇ループへの直接介入こそが、NAD⁺ナドプラ®療法の核心です。
NAD⁺ナドプラ®療法(NMN点滴・NAD⁺点滴・サプリ・点鼻セットなど、NAD⁺を補填・管理する複数の手段を統合した療法)は、枯渇したNAD⁺を直接補充することで、SIRT1・SIRT3の活性回復・PARP1の適正化・ミトコンドリア機能の回復・DNA修復能力の向上・エピゲノムの安定化を同時に目指します。点滴による直接投与はサプリメントと比較してより迅速かつ確実なNAD⁺補充を実現し、慢性的なNAD⁺枯渇ループの断ち切りに有効です。
またWJ幹細胞エクソソーム療法は、NAD⁺枯渇により障害された組織の修復と慢性炎症の抑制をサポートし、NAD⁺枯渇ループの増幅を断ち切るアプローチとして期待されています。