患者さんへの説明
「なぜ年をとると疲れやすくなるのか」——その答えはミトコンドリアにある
私たちの体は約37兆個の細胞でできており、その一つひとつの中に「ミトコンドリア」という小さな発電所があります。ミトコンドリアは食事から得た栄養を燃やして、細胞が動くためのエネルギー(ATP)を作り出しています。
加齢とともに、このミトコンドリアの発電効率が落ちてきます。すると体のあちこちでエネルギー不足が起き、慢性的な疲労感・筋力低下・集中力の低下・代謝の衰えとして現れてきます。これが「老化による疲れやすさ」の正体です。
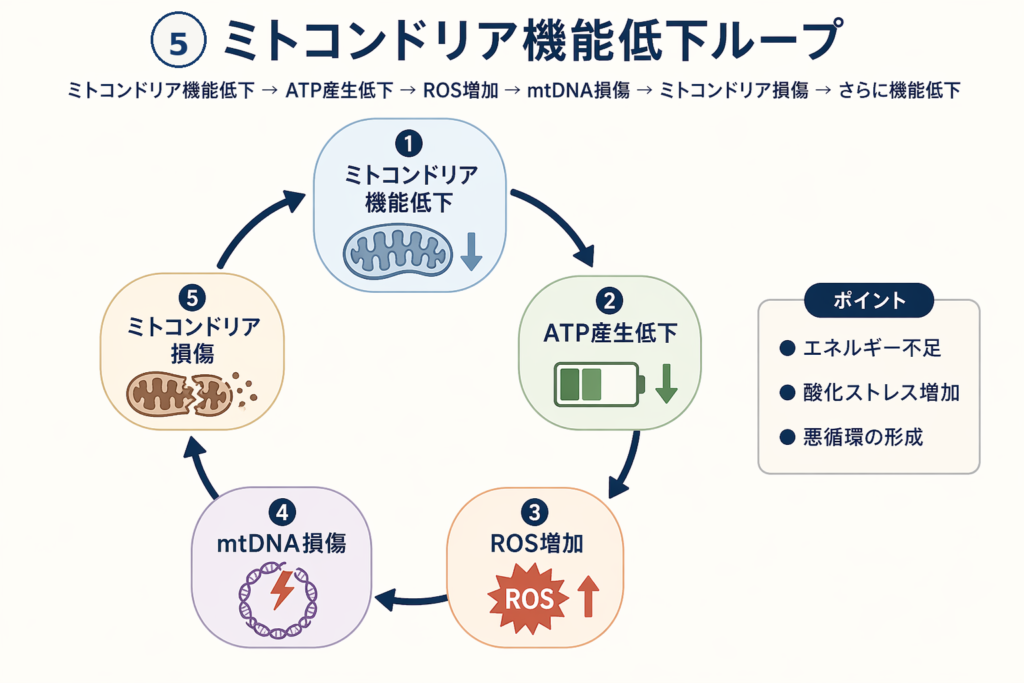
そしてミトコンドリアの機能低下は、それだけでは終わりません。悪循環(ループ)を作り出します:
- ミトコンドリアの効率が落ちる → エネルギー(ATP)が不足する
- 効率が悪くなった発電所から → 活性酸素(ROS)が大量に漏れ出す
- ROSがミトコンドリア自身のDNA(mtDNA)を傷つける → さらに発電効率が落ちる
- mtDNAの修復にNAD⁺が大量消費される → NAD⁺が枯渇する
- NAD⁺が枯渇する → ミトコンドリアの品質管理機能(マイトファジー)が低下する
- 古い・壊れたミトコンドリアが蓄積する → 細胞全体の機能が低下する
- → 最初に戻る(悪循環ループ)
この「ミトコンドリア機能低下ループ」は、慢性疲労だけでなく、心疾患・認知症・糖尿病・筋力低下など多くの老化性疾患の根本に関わっています。ミトコンドリアを守ることは、老化そのものを遅らせることです。
ミトコンドリアの健康を守るために
ミトコンドリアの機能を維持するために最も重要な物質のひとつがNAD⁺(ニコチンアミドアデニンジヌクレオチド)です。NAD⁺はミトコンドリアのエネルギー産生に不可欠な補酵素ですが、加齢とともに体内のNAD⁺量は大幅に減少します。NMNやNAD⁺の補充がミトコンドリア機能の回復に有効とされているのはこのためです。
医師向け:機序の詳細
ミトコンドリア機能低下ループの分子機序
ミトコンドリア機能低下は老化の多くのホールマークと双方向の悪循環を形成します。このループは以下の連鎖で形成されます。
① 電子伝達系(ETC)の効率低下 → ROS産生増加
加齢に伴い、電子伝達系(ETC)複合体I〜Vの活性が低下し、膜電位(ΔΨM)が減少します。ETCの効率低下により電子の漏出が増加し、複合体I・IIIからスーパーオキシドラジカル(O₂⁻)が過剰産生されます。同時に細胞内・ミトコンドリア内のNAD⁺/NADH比が低下し、SIRT3などのNAD⁺依存性脱アセチル化酵素の活性が低下します。
② ROS → mtDNA損傷 → ETC機能のさらなる低下(悪循環)
過剰なROSはヒストンによる保護がなく、かつROS産生源に近接しているmtDNAを優先的に攻撃します。ラット肝細胞では、mtDNAの酸化損傷マーカー(8-ヒドロキシデオキシグアノシン)が核DNAの16倍高いことが報告されています。mtDNA変異はETC複合体タンパク質の発現異常を招き、OXPHOS機能をさらに低下させます。これが「ミトコンドリアフリーラジカル老化理論」の分子的基盤です。
③ mtDNA損傷 → PARP1活性化 → NAD⁺枯渇
mtDNA損傷はPARP1(ポリADPリボースポリメラーゼ1)を活性化し、DNA修復のためNAD⁺を大量消費します。NAD⁺枯渇はSIRT1・SIRT3の活性低下を招き、PGC-1αを介したミトコンドリア生合成シグナルが障害されます。MiDAS(ミトコンドリア機能低下関連老化)研究によれば、NAD⁺の補充によりこの悪循環を予防・逆転できる可能性が示されています。
④ マイトファジー障害 → 機能不全ミトコンドリアの蓄積
PINK1/Parkinを介したマイトファジー(選択的オートファジー)は、機能不全ミトコンドリアを除去する品質管理機構です。NAD⁺枯渇・SIRT1低下・mTOR過活性により、加齢に伴いマイトファジー機能が低下します。脂質代謝の障害により老化細胞に蓄積した脂質ドロップレットがp62依存的にマイトファジーを阻害し、ミトコンドリア機能低下のさらなる悪循環を形成します。
⑤ ミトコンドリア膜透過性遷移孔(mPTP)の開口
酸化ストレス・Ca²⁺過負荷・内膜電位(IMM)脱分極により、mPTPの病的な開口が促進されます。mPTPの全開口は膜電位喪失・ミトコンドリアROS産生増加・Ca²⁺緩衝能低下を引き起こし、悪循環を形成します。加齢に伴いmPTP活性化が亢進し、細胞老化(Senescence)・アポトーシスのトリガーとなります。
⑥ SASP・慢性炎症・細胞老化との連動
機能不全ミトコンドリアはSASP(老化関連分泌表現型)を介して慢性炎症を促進し、周囲の正常細胞に老化を伝播させます(#01慢性炎症ループと連動)。またテロメア短縮とミトコンドリア機能低下は「テロメア-ミトコンドリア-老化軸」として連動しており、p53/PGC-1α経路を介してミトコンドリア生合成をさらに抑制します。
引用論文
- Mitochondrial dysfunction and aging: multidimensional mechanisms and therapeutic strategies. Biogerontology. 2025. PubMed
- Sizek H, et al. Unlocking MiDAS with NAD⁺ – A Boolean model of mitochondrial dynamics and cell cycle control. Transl Oncol. 2024. PubMed
- Wiley CD, Bhaumik D. Mitochondrial dysfunction in cell senescence and aging. J Clin Invest. 2022. JCI
- Bratic A, Larsson NG. Mitochondrial Aging and Age-Related Dysfunction of Mitochondria. J Intern Med. 2013. PubMed
- Mitochondrial DNA Damage and Its Repair Mechanisms in Aging Oocytes. PMC. 2024. PubMed
CyTIXのアプローチ
ミトコンドリア機能低下ループへの介入は、NAD⁺ナドプラ®療法の最も重要な作用機序のひとつです。
NAD⁺ナドプラ®療法(NMN点滴・NAD⁺点滴・サプリ・点鼻セットなど、NAD⁺を補填・管理する複数の手段を統合した療法)は、ループの核心にあるNAD⁺枯渇を直接補充することで、SIRT1・SIRT3の活性回復、PGC-1αを介したミトコンドリア生合成の促進、マイトファジー機能の回復を同時に目指します。MiDAS研究が示すように、NAD⁺の補充はミトコンドリア機能低下関連老化の予防と逆転に最も有望なアプローチです。
またWJ幹細胞エクソソーム療法は、ミトコンドリア機能低下による組織障害を修復し、慢性炎症を抑制するアプローチとして期待されています。