患者さんへの説明
活性酸素には「善玉」と「悪玉」がある
「活性酸素が体に悪い」という話をよく耳にしますが、実は活性酸素(ROS)にはすべてが悪いわけではありません。善玉と悪玉があります。
善玉ROSは体を守るために必要です。細菌やウイルスを撃退したり、細胞同士の情報伝達を助けたり、運動後に筋肉を強くする適応反応を促したりする大切な働きがあります。
問題は「悪玉ROS」、特にヒドロキシルラジカル(·OH)と呼ばれる最も攻撃性の高い活性酸素です。これは体内に分解する酵素がなく、DNA・タンパク質・細胞膜を無差別に攻撃し続けます。
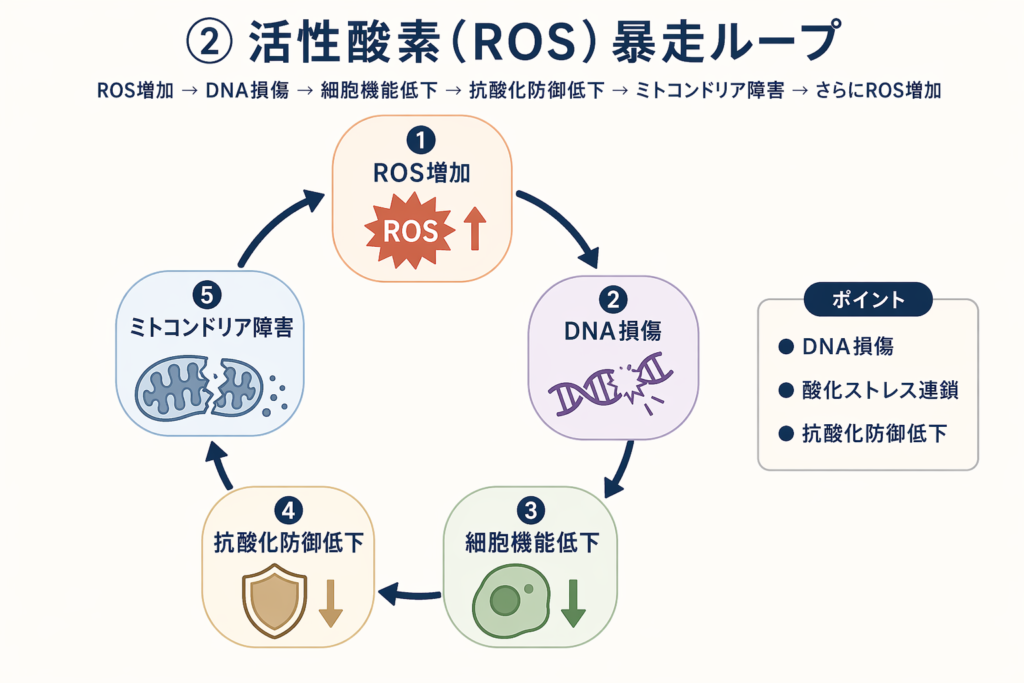
悪玉ROSが「暴走ループ」を作る
加齢とともにミトコンドリアの機能が低下すると、悪玉ROSの産生量が体の抗酸化防御能力を上回ります。するとこんな悪循環が始まります:
- 悪玉ROSが増える → ミトコンドリアが傷つく
- ミトコンドリアが傷つく → さらに悪玉ROSが産生される
- 悪玉ROSがDNAを攻撃する → 修復にNAD⁺が消費される
- NAD⁺が枯渇する → ミトコンドリア機能がさらに低下する
- → 最初に戻る(暴走ループ)
ロンジェビティ医療の目標は「ROSをゼロにする」ことではありません。善玉ROSを守りながら、悪玉ROSの暴走ループを断ち切ることです。
抗酸化療法の選び方 — 水素とビタミンCの違い
抗酸化療法にはいくつかの選択肢があり、それぞれ作用する活性酸素の種類が異なります。
水素(H₂)吸引・点滴は、最も危険な悪玉ROS(ヒドロキシルラジカル)に選択的に作用し、善玉ROSはそのまま残します。分子サイズが極めて小さいため、ミトコンドリアの中まで到達できる点も大きな特徴です。
一方、高濃度ビタミンC点滴は広範な活性酸素に作用しますが、善玉ROSも除去する可能性があります。また高濃度では過酸化水素を介して悪玉ROSであるヒドロキシルラジカルを生成するリスクも指摘されています。
どちらが優れているかではなく、患者さんの状態と目的に合わせて医師が適切に組み合わせることが重要です。
医師向け:機序の詳細
ROS暴走ループの分子機序
生理的レベルのROSはNrf2・NF-κBなどの転写因子を介したレドックスシグナリングに不可欠です(酸化ユーストレス)。しかし加齢に伴いこのバランスが崩れ、病的な酸化ストレス状態へ移行します。このループは以下の連鎖で形成されます。
① ミトコンドリア電子伝達系からのROS産生
加齢に伴いミトコンドリアの電子伝達系(ETC)の効率が低下すると、複合体I・IIIから電子が漏出し、スーパーオキシドラジカル(O₂⁻)が過剰産生されます。O₂⁻はSODによりH₂O₂に変換され、さらに鉄イオンとのフェントン反応により最強の悪玉ROSであるヒドロキシルラジカル(·OH)が生成されます。·OHを分解する内因性酵素は存在しないため、DNA・脂質・タンパク質を無差別に攻撃します。
② ROS → mtDNA損傷 → さらなるROS産生(悪循環)
過剰なROSはミトコンドリアDNA(mtDNA)を直接攻撃し、変異を蓄積させます。損傷したmtDNAは電子伝達系タンパク質の機能をさらに低下させ、より多くのROSを産生するという悪循環を形成します。これが「ミトコンドリアフリーラジカル老化理論」の分子的基盤です。
③ ROS → PARP1活性化 → NAD⁺枯渇
ROSによるDNA損傷はPARP1(ポリADPリボースポリメラーゼ)を活性化し、DNA修復のためにNAD⁺を大量消費します。NAD⁺/NADH比の低下はSIRT1・SIRT3の活性低下を招き、ミトコンドリアの品質管理機能(マイトファジー)をさらに障害します。これがROSループとNAD⁺枯渇ループの連動点です。
④ ROS → NF-κB活性化 → 慢性炎症・細胞老化との連動
過剰なROSはNF-κBシグナルを活性化し、IL-6・TNF-α・IL-1βなどの炎症性サイトカインの産生を促進します。また酸化ストレスはp53・p21経路を介して細胞老化(Senescence)を誘導し、SASP(老化関連分泌表現型)を介して周囲の細胞へ老化を伝播させ、ループ全体を増幅します。
⑤ 抗酸化介入の選択:H₂ vs ビタミンC(医師向け詳細)
H₂(分子状水素)は2007年のOhsawaらの発見以来、ヒドロキシルラジカル(·OH)とペルオキシナイトライト(ONOO⁻)に選択的に作用することが確認されています。H₂の分子量は最小(2g/mol)であり、細胞膜・ミトコンドリア膜・血液脳関門を自由に透過し、最も危険な悪玉ROSに直接作用します。善玉ROS(シグナル伝達に必要なH₂O₂など)は除去しないため、生理的なレドックスバランスを維持できます。
一方、高濃度ビタミンC(アスコルビン酸)はO₂⁻を還元する広範な抗酸化作用を持ちますが、同時にH₂O₂を産生します。体内の遊離鉄(Fe²⁺)とのフェントン反応により·OHが生成されるリスクがあり、特に高濃度投与時はこの点に注意が必要です。がん治療目的の高濃度ビタミンC点滴と水素吸引の併用は、この懸念を補完する合理的なアプローチとして一部クリニックで採用されています。
CyTIXとしては、患者の酸化ストレスの状態・目的・既往歴に応じた個別プロトコル設計を推奨しています。
引用論文
- Bhatt S, et al. Progress in Understanding Oxidative Stress, Aging, and Aging-Related Diseases. Antioxidants. 2024. PubMed
- Shitaw EE, et al. Inter-Organelle Crosstalk in Oxidative Distress: A Unified TRPM2-NOX2 Mediated Vicious Cycle. Antioxidants. 2025. PubMed
- Ohsawa I, et al. Hydrogen acts as a therapeutic antioxidant by selectively reducing cytotoxic oxygen radicals. Nature Medicine. 2007. PubMed
- Bhattacharyya A, et al. Oxidative stress response elicited by mitochondrial dysfunction. Longevity. 2013. PubMed
- Valko M, et al. Reactive oxygen species, toxicity, oxidative stress, and antioxidants. Archives of Toxicology. 2023. Springer
CyTIXのアプローチ
NAD⁺ナドプラ®療法(NMN点滴・NAD⁺点滴・サプリ・点鼻セットなど、NAD⁺を補填・管理する複数の手段を統合した療法)は、ROSループの核心にあるNAD⁺枯渇を直接補充することでPARP1の過剰活性を抑制し、ミトコンドリア機能の回復を目指します。
またWJ幹細胞エクソソーム療法は、酸化ストレスによって傷ついた組織の慢性炎症を抑制し、細胞修復をサポートします。
高濃度ビタミンC点滴については、患者さんの状態と目的に応じて、水素療法との組み合わせも含めた個別プロトコルをご提案します。