米国の厚労省に当たるFDAに申請しておりました、DCF細胞治療の希少病認定(Orphan Drug Designation)が、本日指定されました。
*FDA=U.S.Food & Drug Administrationの略称
*Orphan Drug Designation=開発中の薬や治療法に対し、米国内の患者人口が200,000人以下の疾病に対するものは、市場が限定的とみなされる為に、大手企業が率先して開発しないだろうということから、この分野を担うベンチャー企業に対して有望なものに指定を与え、開発費に対する課税の軽減や、研究開発費を得やすくするような仕組みのこと。
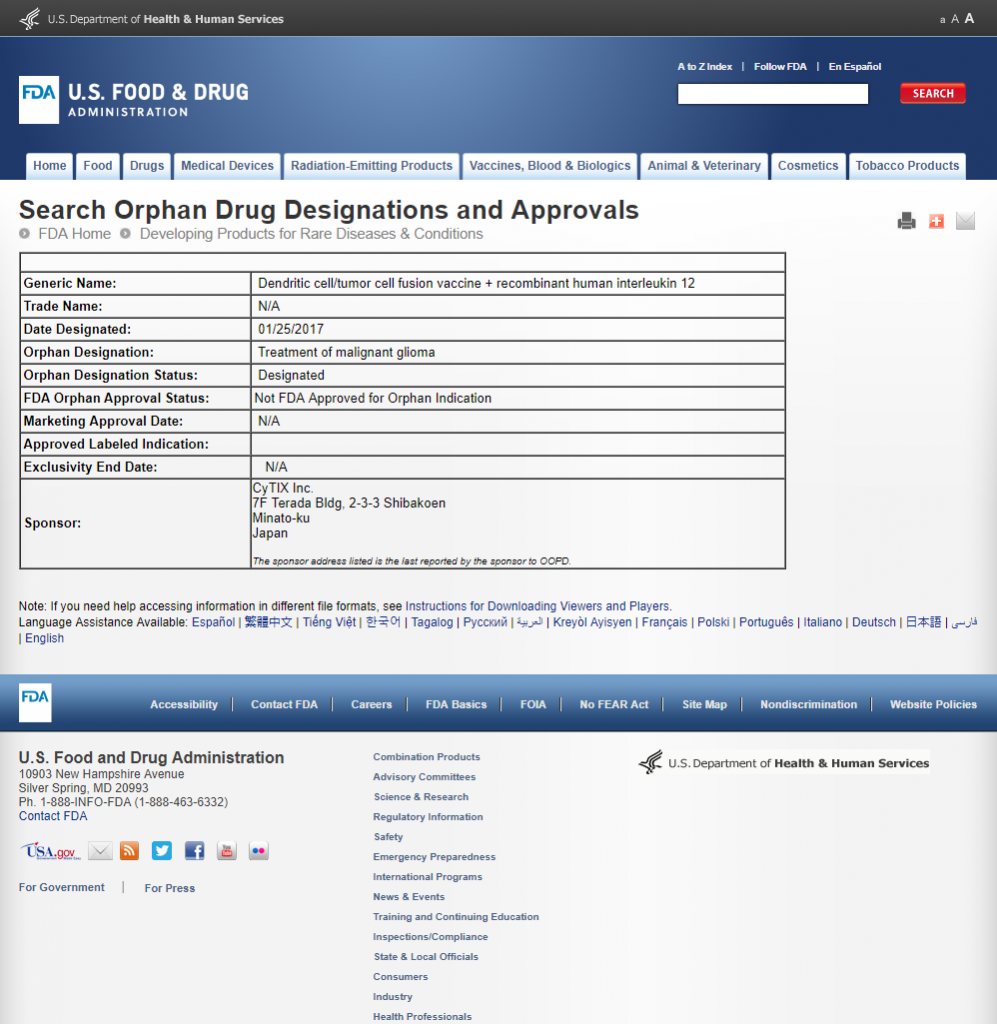
本日(2017年1月25日)、米国FDAより、当社で開発中の「Dendritic cell/tumor cell fusion vaccine + recombinant human interleukin 12」(通称名;DCF細胞治療)が、悪性脳腫瘍の治療法としてOrphan Drug Designationの認定を受けましたのでご報告申し上げます。
当社が出ているFDAのサイトへのリンク⇒ https://www.accessdata.fda.gov/scripts/opdlisting/oopd/detailedIndex.cfm?cfgridkey=552316
 当社は、この認定を大変栄誉あるものであると同時に、DCF細胞治療が有望なものであるという一定のお墨付きを得たものと認識し、更なる治験の枠組みを作るべく今後も活動を継続して参ります。
当社は、この認定を大変栄誉あるものであると同時に、DCF細胞治療が有望なものであるという一定のお墨付きを得たものと認識し、更なる治験の枠組みを作るべく今後も活動を継続して参ります。
[showwhatsnew]
